Cell | 李大鹏研究组破解尼古丁完整生物合成路径
尼古丁是茄科植物特有的高效抗虫物质,自1690年起便作为农药广泛应用于农业生产。同时它对治疗阿尔茨海默病、帕金森病、精神分裂症、抑郁症等精神类疾病也具有重要药用价值。如今,尼古丁已深刻影响了人类历史、农业与植物演化。然而,自1828年尼古丁被首次分离以来,植物如何完成其生物合成的最后步骤,一直是困扰科学界长达近80年的未解之谜。
北京时间2026年4月1日,中国科学院分子植物科学卓越创新中心李大鹏研究团队在国际权威学术期刊《细胞》(Cell)上发表题为“Complete biosynthesis of nicotine”的研究论文。研究团队在北美原住民3000多年前就使用的野生郊狼烟草Nicotiana attenuata中,利用信息论指导的跨尺度多维组学协同分析新技术,首次完整揭示了尼古丁合成路径,并阐明了其中通过酶催化完成碳碳键连接的分子间曼尼希反应的分子机制。该研究揭示了一个由五组分动态代谢通道(metabolon)介导的协同催化与运输机制,破解了这一植物次生代谢与化学防御领域的世纪难题。
研究团队在野生烟草中意外发现一个尼古丁缺失突变体(ao2),并由此锁定了尼古丁吡啶环合成的关键基因NaAO2。进一步通过构建从群体到个体以及单细胞水平等多个尺度的基因组学、转录组学和非靶向结构代谢组学协同分析网络,团队鉴定出一系列参与尼古丁最终合成的关键组分,包括糖基转移酶(NaUGT1)、还原酶(NaA622)、类小檗碱桥酶(NaBBL1/2)、糖苷水解酶(NaBGL1/2)及MATE转运蛋白(NaMATE1)。
研究团队发现植物堪称自然界中的有机合成专家,尼古丁的最终合成并非通过单一“尼古丁合成酶”完成,而是由一个定位于液泡膜的五组分动态代谢通道协同实现。整个过程十分巧妙且隐蔽地采用了“糖基化和去糖基化”机制:烟酸首先通过糖基转移酶(UGT)进行氮原子的糖基化修饰,维持其阳离子状态;随后由还原酶(A622)进行还原并脱羧,对分子进行活化;接着通过一个由类小檗碱桥酶(BBL)连续催化具有立体选择性的分子间曼尼希反应完成与另一个吡咯烷环的分子间缩合以及后续氧化反应;最后经葡萄糖苷水解酶(BGL)进行去糖基化,生成手性纯净的尼古丁,并通过MATE转运蛋白存储于液泡中。这一代谢通道不仅实现了中间产物的高效传递,还避免了有毒中间体的积累,同时防止了高浓度产物对合成途径的反馈抑制,巧妙解决了植物自身防御中的“自毒困境”。
该研究完成了尼古丁生物合成通路的最后一块拼图,揭示了一种由多酶协同催化的立体选择性分子间曼尼希反应机制(该反应被视为许多生物碱合成的“骨架构建”或“关键第一步”)。许多次生代谢合成具有细胞毒性与自抑制作用,该因素是目前制约合成生物学合成效率与大规模应用的重要瓶颈。该研究发现尼古丁天然进化出一条高效“流水线”,既能引导尼古丁高效合成,又能直接将其高活性、手性纯净的产物转运存储于液泡中,巧妙规避了中间体的细胞毒性以及尼古丁对自身合成的反馈抑制。研究提出的“合成与运输偶联”的代谢通道范式,将为突破高价值天然产物生物合成效率瓶颈提供全新的理论依据与工程化策略。
中国科学院分子植物科学卓越创新中心李大鹏研究员为论文通讯作者,常丽静、徐贞、邓普荣、张宁、贺亭瑞为论文共同第一作者。该研究得到了科技创新2030-重大项目、植物性状形成与塑造全国重点实验室、中国科学院先导专项、国家重点研发计划、国家自然科学基金等项目的资助。
论文链接:https://doi.org/10.1016/j.cell.2026.03.034
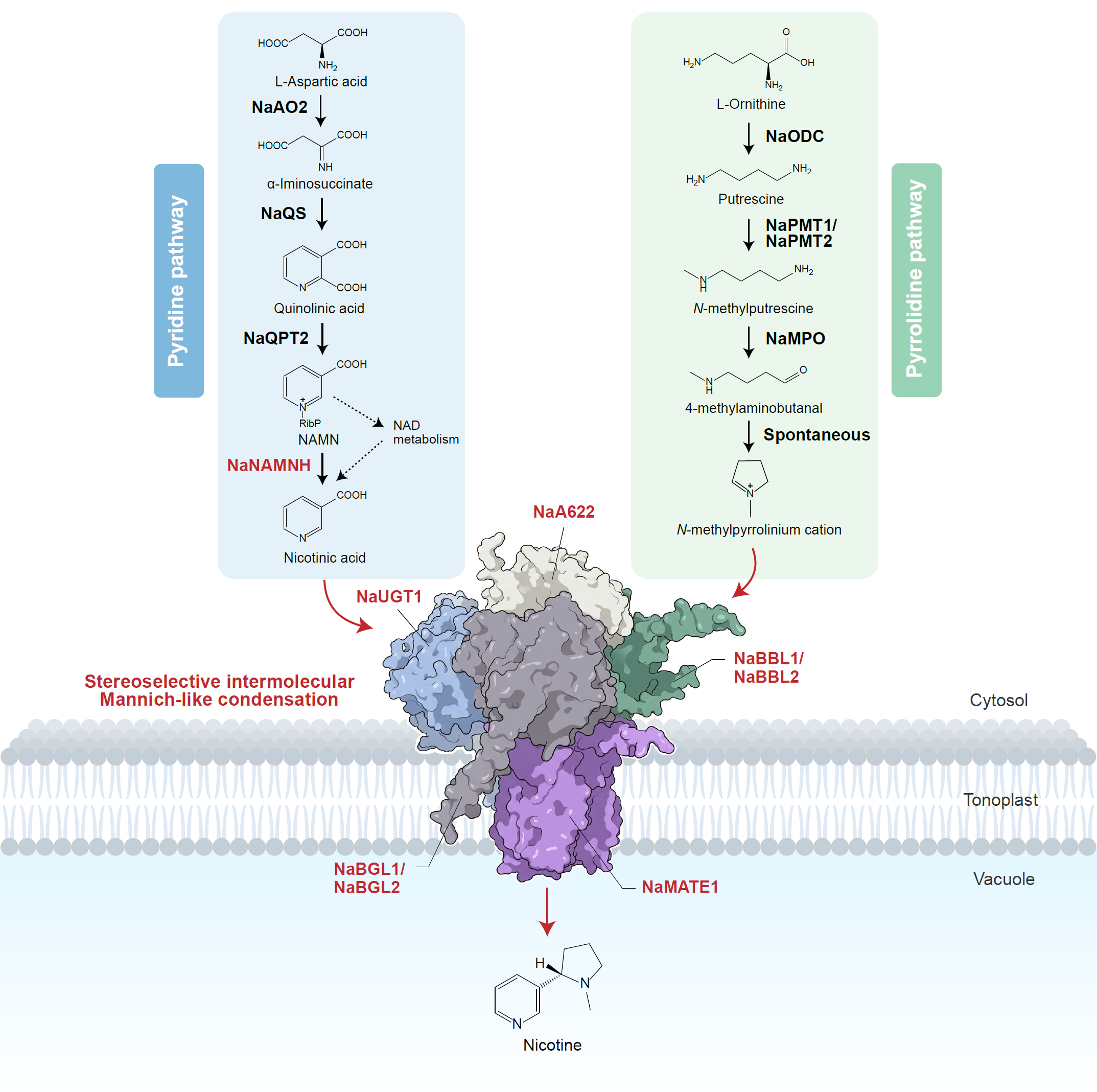
尼古丁完整合成通路