李建戌研究组揭示黄酮合成关键调控机制,为作物改良提供新策略
2026年3月14日,Nature Communications在线发表了中国科学院分子植物科学卓越创新中心辰山科学研究中心李建戌研究组题为“Molecular mechanism underlying regulation of chalcone synthase by chalcone isomerase-like protein”的研究论文。该研究首次解析了植物黄酮类化合物生物合成途径关键酶—查尔酮合酶(Chalcone synthase,CHS)与IV型查尔酮异构酶(chalcone isomerase-like protein,CHIL)形成的蛋白复合体高分辨率三维结构,阐释了CHIL调控CHS催化效率与产物特异性的分子机制,为深入理解植物次生代谢流的精准调控提供了重要见解。
黄酮类化合物是植物体内一类至关重要的次生代谢产物,在植物生长发育、逆境适应中发挥关键作用,同时因其显著的抗氧化、抗炎、抗菌、抗病毒等生理活性而具有重要的食用和药用价值。作为黄酮类化合物生物合成途径中的第一个关键限速酶,查尔酮合酶(CHS)负责将代谢流从苯丙烷途径引导到黄酮代谢途径。然而,CHS本身存在“催化混杂性”,在酶活反应中能生成大量副产物,从而限制了黄酮类化合物的合成效率。此前研究发现,CHIL可以与CHS发生相互作用并调控其酶学特性,但具体的分子机制并不清楚。
为解决这一科学问题,研究人员成功解析了CHS-CHIL蛋白复合体的高分辨率晶体结构,结合生物化学分析与分子动力学模拟,逐步揭示了其调控机制。结构与生化分析显示,CHIL通过其-发卡结构控制底物结合口袋入口的开关,从而调控CHS的功能。分子动力学拟结果表明,CHIL对CHS产物特异性的调控可能发生在催化循环的早期阶段,比如底物结合或中间体形成阶段。CHIL借助-发卡结构,通过促进辅酶 A的释放并协助CHS内部关键氨基酸残基的正确定位,增强CHS的酶活性与产物特异性。研究进一步揭示了位于CHIL 蛋白β-发卡结构上的关键功能位点—His36的重要作用,在拟南芥及多种植物中将该组氨酸突变为亮氨酸后,CHS的催化效率与产物特异性得到进一步提升。
研究人员还追溯了CHIL蛋白的进化过程,对从苔藓到被子植物的多种陆生植物CHIL同源蛋白进行了系统分析,证实该分子调控机制在陆地植物演化过程中高度保守。基于进化分析结果,团队成功设计出CHIL 的突变体 H36E/F37T,该突变体在增强CHS酶活性、提升黄酮类化合物合成效率方面表现出优异性能。考虑到黄酮类化合物不仅是作物营养品质的核心指标,也是植物抵抗逆境胁迫的关键因素,这一调控机制的强化可以为作物适应复杂环境、提升营养品质提供了关键的分子改良靶点。
该研究是李建戌研究团队在植物次生代谢调控领域取得的重要进展。研究揭示的CHS-CHIL复合体结构与分子调控机制信息,不仅回答了该领域长期存在的关键科学问题,深化了对黄酮代谢流调控核心元件的认知,也为未来通过分子设计改良作物黄酮类化合物的含量与组成、培育优质抗逆新品种提供了直接的理论指导和潜在的蛋白工程改造靶点。
中国科学院分子植物科学卓越创新中心辰山科学研究中心的研究生王淞、科研助理马立莹和分子植物科学卓越创新中心的徐洲更博士为该论文的共同第一作者,李建戌研究员为该论文的通讯作者。上海师范大学的俞芳副研究员,分子植物科学卓越创新中心的王佳伟研究员、张鹏研究员、朱木兰研究员、郝洁副研究员和马妙莲正高级实验师,山东大学的程爱霞教授,上海辰山植物园的许晶晶副研究员等也参与了研究和讨论。该研究得到了国家自然科学基金、上海市农业科技创新项目以及上海市绿化和市容管理局科学技术项目等的资助。
论文链接:https://www.nature.com/articles/s41467-026-70563-4

图1:CHS-CHIL复合体的结构与功能。
a-b:IV型查尔酮异构酶(chalcone isomerase-like protein,CHIL)可以调控查尔酮合酶(Chalcone synthase, CHS)的催化效率与产物特异性;c:CHS-CHIL复合体的晶体结构。
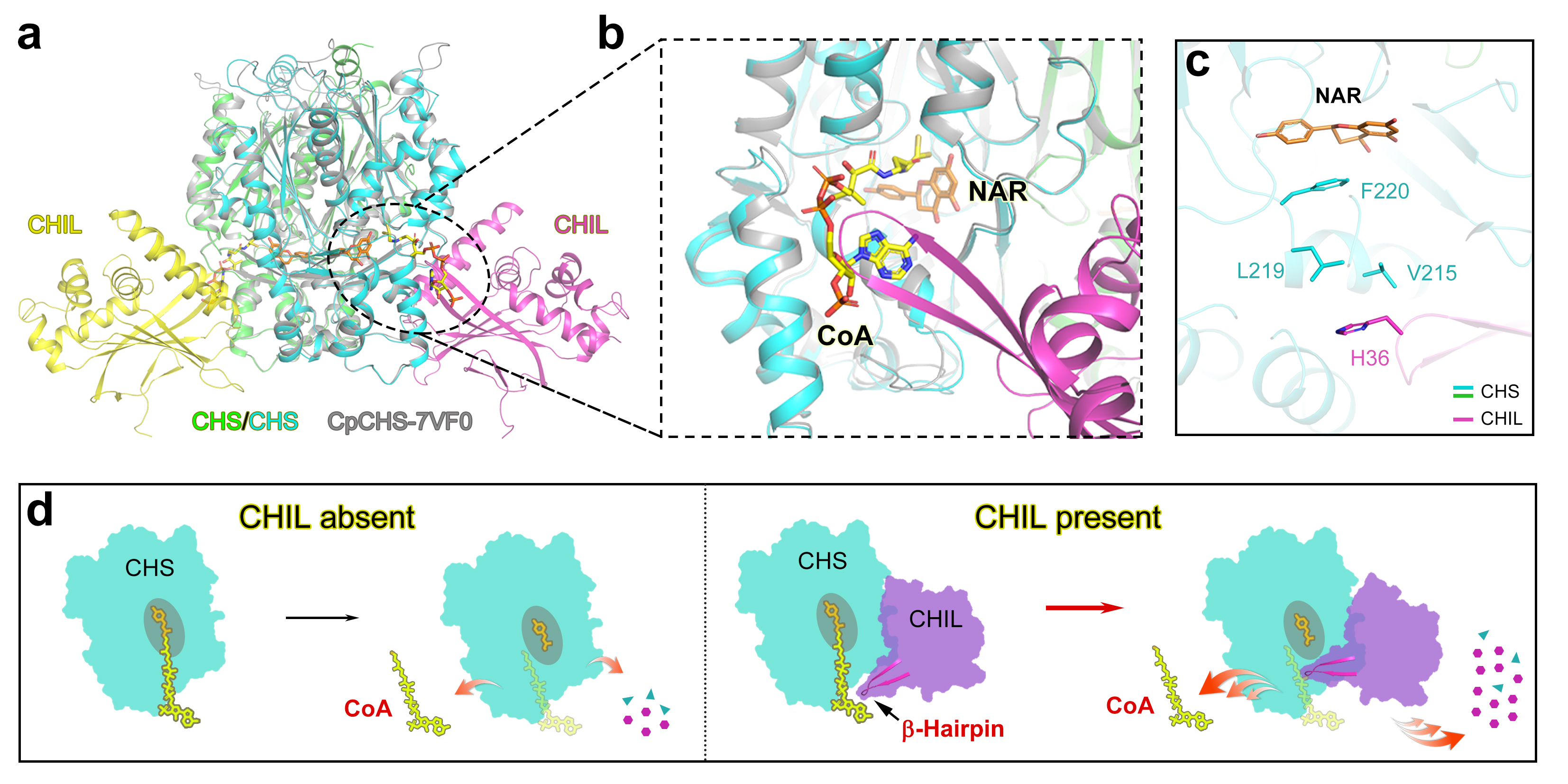
图2:CHIL调控CHS活性的分子机制。
在没有CHIL结合时,CHS的催化效率较低,且因产物CoA释放缓慢而产生更多副产物;当CHIL与CHS结合后,其-Hairpin结构不仅能加速CoA释放,还可以稳定CHS活性位点的正确构象,所以CHS的催化效率显著提高,副产物大大减少。