赵国屏研究组发现CRISPR/Cas12a切割ssDNA的新活性
2018年3月12日, 《Cell Research》杂志在线发表了我所赵国屏研究组题为“Cas12a兼具顺式和反式单链DNA切割活性”(CRISPR-Cas12a has both cis- and trans-cleavage activities on single-stranded DNA)的最新研究论文。本文深入系统地研究了Cas12a对于靶标单链DNA和非靶标单链DNA的切割特性。
作为生命的基本遗传物质,DNA的精准编辑和快速检测一直以来都受到高度的重视。近年来,随着CRISPR/Cas9系统的发现和开发,人们对基因治疗重新燃起了新希望;尽管存在一些潜在的安全风险和一定的伦理之争,CRISPR/Cas9系统出于其相对精准和高效,已经开始被应用于临床的研究。与此同时,科学家也开始将CRISPR系统引入核酸快速检测领域,期望为现有的临床诊断技术带来突破。
在本研究中,作者发现Cas12a在靶标ssDNA的第22位附近特异切割DNA(称为cis切割),并且该切割行为不需要PAM序列的辅助。同时,研究还发现,一旦Cas12a与crRNA以及靶标DNA形成三元复合体后,该复合物就会显示出很强的“乱切”活性,并将体系中任意单链DNA切成碎片(称为trans切割)。借助于质谱分析,作者发现Cas12a将ssDNA切成2-4nt的片段。根据一系列点突变的实验结果,作者还证明了Cas12a的cis和trans切割活性都和其RuvC口袋(‘RuvCpocket’)相关,并据此提出了Cas12a切割ssDNA的分子模型。该研究成果有望为DNA临床诊断提供新的研究思路。
赵国屏研究组近年来聚焦于合成生物学使能技术的开发和应用,开发了多项DNA编辑和检测的方法,并积极推动这些方法用于临床研究。该研究得到了中国科学院先导专项(“人工染色体构建与稳定遗传的技术方法”)、中国科学院青年创新促进会和国家自然科学基金委的经费资助。
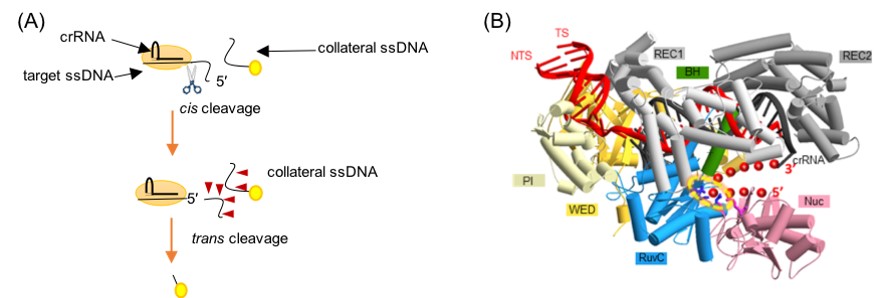
图1. CRIPSR/Cas12a切割单链DNA的示意图(A)和三元复合物的结构模拟图(B)。